Eine vollständige Liste der US-amerikanischen Kolleginnen und Kollegen des zuständigen ADA-Fachausschusses, die diese Leitlinien jährlich unter Berücksichtigung der aktuellen Evidenz aktualisieren, findet sich am Ende der Einleitung der SoC. Hervorzuheben dabei ist, dass sich die SoC konsequent an der jeweils verfügbaren Evidenzlage orientieren, und besonders bemerkenswert ist, dass diese zeitintensive Arbeit neben den klinischen Verpflichtungen der Beteiligten geleistet wird.
Um Veränderungen gegenüber dem Vorjahr schneller erfassen zu können, enthält das Werk ein eigenes Kapitel, in dem relevante Neuerungen gezielt herausgestellt werden. Die SoC enthalten unter anderem wichtige Anpassungen für mehrere Medikamentenklassen. So wird der Einsatz von GLP-1-Rezeptoragonisten sowie dualen GIP/GLP-1-Rezeptoragonisten unter anderem auf HFpEF, CKD, MASLD und MASH ausgeweitet. Im Abschnitt Insulin Administration Technique freut es den Autor dieses Beitrags, dass die Empfehlungen der FITTER-Forward-Expertengruppe als Referenz für ein optimales Vorgehen bei der Insulinapplikation hervorgehoben werden.
Änderungen bei Diabetes-Technologie mit aktualisierten Empfehlungen
Zu den zentralen Aktualisierungen im Bereich der Diabetes-Technologie zählen die folgenden Punkte (Kapitel 7: Diabetes Technology: Standards of Care in Diabetes – 2026; Tabelle 1):
- Ausweitung der Verlaufskontrolle auf alle Diabetes-Typen
- Nutzung von CGM-Daten zur Überwachung des Krankheitsverlaufs bei präsymptomatischen Menschen mit Typ-1-Diabetes (T1D)
- stärkere Betonung des Einsatzes von CGM- und AID-Systemen für alle Altersgruppen und alle Stadien des Diabetes
- Empfehlungen zu AID-Systemen, die allen Erwachsenen mit T1D sowie Menschen mit Typ-2-Diabetes (T2D), die Insulin erhalten, angeboten werden sollen.
Im weiteren Text wird ausgeführt, dass die Vorteile von CGM unabhängig von Alter, Geschlecht, Bildungs- oder Einkommensniveau sowie von den Ausgangsmerkmalen des Diabetes nachgewiesen sind. Auffällig ist zudem eine terminologische Weiterentwicklung: Begriffe wie isCGM werden zunehmend nicht mehr verwendet. Stattdessen ist von rtCGM oder allgemein von CGM die Rede. Diese Entwicklung spiegelt die Veränderungen im CGM-Ökosystem der vergangenen zehn Jahre wider und findet nun auch konsequent Eingang in die SoC-Terminologie.
Änderungen bei den Empfehlungen in den SoC im Vergleich zum Vorjahr
- Es wurden Empfehlungen hinsichtlich der Aufklärung und Schulung von Menschen mit Diabetes und medizinischem Fachpersonal (HCP) je nach Art des Geräts hinzugefügt, wobei sogar Details zur Aufklärung und Schulung je nach Art des Geräts angegeben werden. Zu den wichtigsten Aktualisierungen gehören Inhalte über die Unterstützung, die die HCP möglicherweise benötigen.
- Die Empfehlung 7.3 wurde in zwei Empfehlungen unterteilt und enthält Leitlinien zur Verschreibung und Nutzung von CGM-/AID-Systemen. Die Empfehlung 7.3a befasst sich mit der Verschreibung, Einführung und Überwachung eines CGM-Systems, während Empfehlung 7.3b dieselben Aspekte für Systeme zur automatisierte Insulindosierung (AID) beschreibt.
- Die Empfehlung 7.6 wurde geändert, um Kinder und Jugendliche in der Schule bei der Verwendung von Diabetes-Technologie wie CGM-Systemen, kontinuierlicher subkutaner Insulininfusion (CSII), vernetzten Insulinpens und AID-Systemen zu unterstützen. Ältere Schüler (≥18 Jahre) werden in der neuen Empfehlung 7.7 behandelt, in der auch Anpassungen am Arbeitsplatz diskutiert werden. Die Empfehlung 7.7 für Personen ≥18 Jahre besagt, dass für Erwachsene mit Diabetes, die Diabetes-Technologie verwenden, angemessene Anpassungen im Bildungs- und Arbeitsumfeld für ausreichend Zeit für die Nutzung ihrer Systeme und die Reaktion auf hohe und niedrige Glukosewerte umfassen sollte.
- Die Empfehlung 7.8 befasst sich mit der frühzeitigen Einführung aller Systeme, je nach den Umständen des jeweiligen Nutzers. Die neue Empfehlung 7.8a besagt, dass vor dem Beginn der Nutzung von CSII oder AID keine Anforderungen hinsichtlich der Höhe des C-Peptid-Spiegels, des Vorhandenseins von Inselautoantikörpern oder der Dauer der Insulinbehandlung gestellt werden sollten.
- Der Abschnitt „Blutzuckermessung” enthält aktualisierte Literatur, in der die Vorteile der Blutglukosemessung für Menschen mit T2D hervorgehoben werden. Darüber hinaus wird darin betont, wie wichtig es ist, dass Personen, die CGM verwenden, auch Zugang zu Blutglukosemessungen haben.
- Die Empfehlung 7.15 besagt, dass die Verwendung von CGM nun bei Diagnose der Diabeteserkrankung und jederzeit danach für Kinder, Jugendliche und Erwachsene mit Diabetes empfohlen wird, die eine Insulintherapie, eine Nicht-Insulin-Therapie, die zu Hypoglykämien führen kann, oder eine andere Diabetestherapie erhalten, bei der CGM diese unterstützt.
- Die Empfehlung 7.17 befasst sich kurz mit der Verwendung von Diabetesgeräten in der Schwangerschaft, die in Kapitel 15 der SoC ausführlich behandelt wird.
- Die Empfehlung 7.25a besagt, dass AID-Systeme das bevorzugte Insulinabgabesystem für Menschen mit T1D und Erwachsene und Kinder mit T2D sind, die mehrere tägliche Injektionen, CSII oder eine sensorgestützte Pumpentherapie erhalten, sowie für andere Formen von insulinabhängigem Diabetes.
- Die Empfehlung 7.25b besagt, dass AID-Systeme bei Menschen mit T2D, die Basalinsulin erhalten und ihre individuellen Blutzuckerziele nicht erreichen, in Betracht gezogen werden können.
Kostenerstattung für CGM-Systeme bei Menschen mit Typ-2-Diabetes und Insulintherapie – Definitionen der intensivierten Insulintherapie
Ein Aspekt der SoC ist aus deutscher Perspektive aus aktuellem Anlass von besonderem Interesse: die Kostenerstattung für CGM-Systeme bei Menschen mit T2D, die eine „intensivierte Insulintherapie“ durchführen. Zwischen den USA und Deutschland (sowie anderen europäischen Ländern) bestehen hierbei Unterschiede hinsichtlich dessen, was unter einer solchen Therapie verstanden wird – insbesondere in Bezug auf verwendete Begriffe und deren Definitionen (Tabelle 1).
So ist Multiple Daily Injections (MDI) in den USA ein etablierter Standardbegriff. Diese Form der Insulintherapie wurde in der überwiegenden Mehrzahl der klinischen Studien zum Nutzen von CGM bei dieser Nutzergruppe eingesetzt. Die Evidenzbasis für den Einsatz von CGM bei Menschen mit T2D unter intensivierter Insulintherapie beruht daher weitgehend auf Daten aus dieser Population.
Darüber hinaus ist zu berücksichtigen, dass selbst bei identischer Terminologie in verschiedenen Ländern nicht zwangsläufig von einer einheitlichen Umsetzung in der klinischen Praxis ausgegangen werden kann. So unterscheiden sich beispielsweise die Inhalte und praktischen Ausgestaltungen dessen, was unter dem Begriff „basalunterstützte orale Therapie (BOT)“ verstanden wird, je nach Land teils erheblich.
Tabelle 1 Begriffsdefinitionen und Regime‑Taxonomie (ICT, SIT, CT)
|
Regime |
Leitliniennahe Kurzdefinition |
Abgrenzungskriterien |
Schulung/Kompetenz |
Primäre Quellen |
|
ICT / CSII |
Basal–Bolus‑Regime mit ≥3 Injektionen/Tag (MDI) oder Insulinpumpe; flexible Mahlzeitenwahl; eigenverantwortliche Dosierung |
KH‑Schätzung/Korrekturfaktoren; SMBG/CGM; individuelle Mahlzeitengestaltung |
Intensive strukturierte Schulung (FIB); funktionelle Insulintherapie |
G‑BA/MVV‑RL; DDG S3; ADA SoC; AACE; IQWiG |
|
SIT (supplementär/ standardisiert) |
Prandiales Insulin ergänzend zur oralen Therapie, überwiegend fixe Dosisschemata; partielle Anpassungen möglich |
Keine volle Basal–Bolus‑Flexibilität; indikationsbezogene Mahlzeitenanpassungen |
Basis‑Schulung; Dosisschemata und Hypoglykämie-Prävention |
NVL v3.0 (Regimenbeschreibung); IQWiG |
|
CT (konventionell) |
Mischinsulin 1–2x/Tag; feste Essenszeiten; geringe Anpassungsspielräume |
Starres Schema; erhöhte Hypoglykämie-Risiken bei variablen Tagesabläufen |
Grundschulung SMBG; Fokus Hypoglykämie-Prävention |
NVL v3.0; IQWiG |
Tabelle 2 Definitionen von „intensiver“ Insulintherapie in verschiedenen Leitlinien und Ländern
- In ADA Standards of Care 2025 wird die intensive Insulintherapie definiert als: „Treat most adults with type 1 diabetes with continuous subcutaneous insulin infusion or multiple daily doses of prandial (injected or inhaled) and basal insulin.“ Quelle: ADA SoC 2025 (Section 9)
- Die AACE 2021/2022 – CGM bei intensiver Insulintherapie: „CGM is strongly recommended for all persons with diabetes treated with intensive insulin therapy, defined as 3 or more injections per day or the use of an insulin pump.“ Quelle: AACE Guideline (Use of Advanced Technology / Clinical Practice Guideline 2022)
- In der Nationalen Versorgungsleitlinie (NVL) v3.0 (2023) – CT Wortlaut: „Konventionelle Insulintherapie (CT): 1–2 Injektionen eines Kombinationsinsulins in fester Mischung.“ Quelle: NVL Typ‑2‑Diabetes – Langfassung, Version 3.0 (Tabelle Formen der Insulintherapie)
- In der NVL v3.0 (2023) – Regimen mit prandialen Zusatz (SIT = supplementäre Insulin Therapie, ‑Äquivalenz): „Empfehlung zur Eskalation der Insulintherapie: Kombination aus Basalinsulin und kurzwirksamen Insulin (ggf. als Mischinsulin).“ Quelle: NVL-Typ‑2‑Diabetes – Langfassung, Version 3.0 (Algorithmus Insulintherapie)
Kostenbeschluss des G-BA aus dem Jahr 2016 zur Kostenerstattung von CGM-Systemen
In Deutschland wird traditionell eine andere Definition der Insulintherapie zugrunde gelegt. So definiert die DDG-S3-Leitlinie „Therapie des Typ-1-Diabetes“ aus dem Jahr 2018 die intensivierte konventionelle Insulintherapie (ICT) wie folgt:
„Die intensivierte Insulintherapie ist definiert als Gabe von mindestens drei Insulininjektionen pro Tag mit getrennter Substitution von Basis- und Mahlzeiteninsulin (Basal-Bolus-Prinzip).“
In anderen Ländern und Leitlinien finden sich zum Teil abweichende Definitionen (Tabelle 2). Die im Beschluss des Gemeinsamer Bundesausschuss (G-BA) aus dem Jahr 2016 festgelegte Definition der intensivierten Insulintherapie (ICT), die Voraussetzung für eine Kostenerstattung von CGM-Systemen ist, ist vergleichsweise präzise formuliert:
„Als intensiviert ist eine Insulintherapie anzusehen, bei der die Patientin oder der Patient entsprechend ihres oder seines Lebensstils den Zeitpunkt und die Zusammensetzung der Mahlzeit selbst frei festlegt und dementsprechend die Dosierung des Mahlzeiteninsulins anhand der Menge der aufzunehmenden Kohlenhydrate und der Höhe des präprandialen Blutzuckerspiegels steuert.“
Der G-BA-Beschluss unterscheidet dabei nicht zwischen Menschen mit T1D und T2D. Dies bedeutet jedoch nicht, dass diese Definition in der Versorgungspraxis strikt angewendet wurde – auch nicht seitens der Krankenkassen. Vielmehr erfolgte die Kostenerstattung vergleichsweise großzügig bei Menschen mit Diabetes, sofern eine intensivierte Insulintherapie in irgendeiner Form durchgeführt wurde (z.B. Fixe Dosierung des Mahlzeiteninsulins mit Nachspritzschema). Nebenbei bemerkt: Im Sommer dieses Jahres jährt sich dieser G-BA-Beschluss zum zehnten Mal.
Weiterentwicklung der Evidenz
Zu berücksichtigen ist, dass sich die Evidenzlage zum Nutzen von CGM-Systemen in den letzten zehn Jahren deutlich weiterentwickelt hat, insbesondere bei der Anwendung durch Menschen mit T2D. Zum Zeitpunkt des GBA-Beschlusses im Jahr 2016 lagen kaum Studien zu dieser Nutzergruppe vor. Diese Weiterentwicklung der Evidenz wird in den aktuellen SoC der ADA deutlich reflektiert, findet jedoch bislang keine Entsprechung in der deutschen Erstattungssituation.
In Deutschland scheint es derzeit vermehrt zu Ablehnungen der Kostenübernahme bei Menschen mit T2D zu kommen, wobei sich die Begründung häufig auf die Art der jeweils durchgeführten intensivierten Insulintherapie stützt. Strukturell fehlt in Deutschland ein verbindendes Element zwischen den jährlich aktualisierten Praxisempfehlungen der Deutschen Diabetes Gesellschaft (DDG), die primär Expertenempfehlungen darstellen, jedoch in der Regel keine expliziten Angaben zum Evidenzniveau enthalten, und den evidenzbasierten Leitlinien der DDG. Letztere beruhen auf einer systematischen Aufarbeitung der Literatur unter Berücksichtigung der verfügbaren Evidenz, werden jedoch nur in mehrjährigen Abständen aktualisiert.
Gerade in einem sich dynamisch entwickelnden Forschungs- und Therapiebereich wie der Diabetes-Technologie ist diese zeitliche Verzögerung problematisch. Für grundsätzlich verfügbare technologische Lösungen fehlen damit in Deutschland häufig aktuelle, belastbare Aussagen medizinischer Fachgesellschaften zur medizinischen Notwendigkeit und zur Evidenzlage. Auf solche Aussagen könnten sich Hersteller – etwa von CGM-Systemen – in Verhandlungen mit Kostenträgern zur Kostenerstattung beziehen, sie stehen derzeit jedoch nur eingeschränkt zur Verfügung. Dabei könnte und sollte der Weg folgendermaßen aussehen: Studienergebnisse aus geeigneten Studien, um die Evidenz nachzuweisen, daraus folgt dann die medizinisch/klinische Empfehlung durch die Fachgesellschaften und deren Experten als relevante Kompentenzgruppe. Hieraus ergibt sich die Umsetzung in Versorgungskonzepte und -modelle.
In Deutschland haben wir aber das Problem dahingehend, dass es für Versorgungkonzepte und -modelle keine belastbaren Aussagen und keine entsprechenden Empfehlungen, geschweige denn Leitlinien gibt. Deren Aktualisierung braucht viele Jahre, während ADA-Empfehlungen jährlich aktualisiert werden.
Vulnerable Nutzergruppen
Ein weiterer relevanter Aspekt ist der Nutzen von CGM-Systemen bei sogenannten „vulnerablen“ Nutzergruppen. Dazu zählen beispielsweise ältere Menschen mit T2D oder Menschen mit Diabetes, die im häuslichen Umfeld gepflegt werden. Für diese quantitativ bedeutsamen Nutzergruppen liegt bislang nur wenig Evidenz aus klassischen klinischen Studien vor – insbesondere unter Berücksichtigung der spezifischen Rahmenbedingungen des deutschen Gesundheitssystems.
Heterogenität der Kostenerstattung in Deutschland
Bei der Bereitschaft zur Kostenerstattung von CGM-Systemen bestehen offenbar Unterschiede zwischen den einzelnen KV-Bereichen in Deutschland. Konkrete, systematisch erhobene Daten hierzu liegen jedoch nicht vor. Diese Heterogenität in der Erstattungspraxis kann unter anderem durch Unterschiede in der Umsetzung von Beurteilungsvorgaben durch die regionalen Medizinischen Dienste bedingt sein, obwohl es eine übergeordnete Vorgabe durch den Medizinischen Dienst gibt.
Heterogenität der Kostenerstattung in Europa
In diesem Zusammenhang sind auch die Unterschiede zwischen den europäischen Ländern hinsichtlich der Kostenerstattung von CGM-Systemen bei Menschen mit T2D und Insulintherapie von Interesse. Diese beruhen de facto auf derselben Evidenzlage, führen jedoch zu teils sehr unterschiedlichen Erstattungsentscheidungen. Eine systematische, vergleichende Übersicht zur CGM-Kostenerstattung in Europa liegt bislang nicht vor.
Die jährlich vom dt-report gelieferten Angaben ermöglichen jedoch bereits heute vergleichende Aussagen für Länder der DACH-Region sowie für Spanien. Perspektivisch wird dies für eine deutlich größere Zahl europäischer Länder möglich sein. Aktuell befindet sich ein Index in der Entwicklung, der einen länderübergreifenden Vergleich der Nutzbarkeit von Diabetes-Technologie ermöglichen soll – in Analogie zum Big-Mac-Index, der Unterschiede in der wirtschaftlichen Leistungsfähigkeit verschiedener Länder veranschaulicht
DMP – aktualisierte Leitliniensynopse des G-BA
Eine Aktualisierung des Disease-Management-Programms (DMP) Diabetes mellitus Typ 2 steht an. Nach Einschätzung des Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) stimmen die bestehenden Regelungen dieses DMP weitgehend mit den Empfehlungen aktueller Leitlinien überein. Im Auftrag des Gemeinsamen Bundesausschusses (G-BA) wurden insgesamt 1.025 Empfehlungen aus 18 aktuellen, evidenzbasierten Leitlinien mit den Regelungen des bestehenden DMP abgeglichen, um den Aktualisierungsbedarf systematisch zu prüfen.
Die Evidenzlage ist konsistent: Der Einsatz von CGM verbessert den HbA1c-Wert, erhöht die Time-in-Range (TIR) und reduziert Hypoglykämien bei insulinbehandelten Menschen mit T2D. Die IQWiG-Leitliniensynopse (V24-11, 13.10.2025) weist CGM als eigenständigen Versorgungsaspekt (K1) aus und identifiziert zugleich eine Diskrepanz zur aktuell gültigen DMP-Anlage (DMP-A-RL). Das Zielbild sieht eine Aufnahme von CGM in das DMP für folgende Gruppen vor:
1. Menschen mit ICT oder CSII sowie
2. Menschen mit MDI bei Vorliegen eines Hypoglykämierisikos, einer Hypoglykämie-Wahrnehmungsstörung oder einer eingeschränkten Fähigkeit zur Selbstmessung (SMBG).
In der medizinisch-wissenschaftlichen Vorbemerkung (MVV) wird ICT dabei als Basal-Bolus-Therapie mit mindestens drei Injektionen pro Tag definiert, CSII als Pumpentherapie mit flexibler Bolus-Anpassung.
Der G-BA ist verpflichtet sicherzustellen, dass bestehende DMPs dem „aktuellen Stand der medizinischen Wissenschaft“ entsprechen. Ziel ist es, Versorgungsqualität, Behandlungsstandards und Dokumentation kontinuierlich an neue medizinische Erkenntnisse und Leitlinien anzupassen. Vor diesem Hintergrund stellt die Leitliniensynopse des IQWiG die zentrale fachliche Grundlage für eine Aktualisierung des DMP dar und sollte im Verfahren das höchste Gewicht haben. Die im Rahmen des Verfahrens vorgesehenen Anhörungen dienen in der Regel der Klarstellung und der Einordnung in den deutschen Versorgungskontext.
In der derzeit gültigen DMP-Regelung wird lediglich eine „angemessene Stoffwechselselbstkontrolle“ erwähnt, die implizit als Selbstkontrolle mittels kapillärer Blutzuckermessung verstanden wird. Der Einsatz von CGM ist hingegen nicht explizit geregelt. Dies führt zu Versorgungsungleichheiten, da insbesondere Menschen mit T2D unter ICT – etwa bei einem festen Spritzschema – auf dieser Grundlage bei einigen Krankenkassen bzw. durch deren Medizinische Dienste von der Kostenübernahme für CGM ausgeschlossen werden.
Die kürzlich publizierte Auswertung internationaler medizinischer Leitlinien durch das IQWiG kommt zu dem Ergebnis, dass CGM für folgende Patientengruppen den evidenzbasierten Versorgungsstandard darstellt:
- Menschen mit intensivierter Insulintherapie (≥3 Insulininjektionen täglich oder Nutzung einer Insulinpumpe) und
- Menschen mit mehreren täglichen Insulininjektionen bei Auftreten von wiederkehrenden oder schweren Hypoglykämien, Hypoglykämie-Wahrnehmungsstörungen oder einer Erkrankung oder Beeinträchtigung, die eine selbstständige kapilläre Blutzuckermessung nicht ermöglicht.
Der G-BA-Beschluss aus dem Jahr 2016 sowie die aktuell gültige DMP-Regelung bilden diese Erkenntnisse bislang nicht ab. Auch eine Stakeholder-Anhörung zeigte eine klare Zustimmung zur Modernisierung des DMP. Eine Anpassung des DMP für die genannten Zielgruppen ist daher medizinisch notwendig, praktisch umsetzbar und versorgungspolitisch konsistent.
Entsprechend sollte CGM in das DMP aufgenommen werden für Menschen mit T2D, die
- eine intensivierte Insulintherapie durchführen (≥3 Injektionen täglich oder Nutzung einer Insulinpumpe), oder
- mehrere tägliche Insulininjektionen erhalten und bei denen mindestens eines der folgenden Kriterien vorliegt:
- wiederkehrende oder schwere Hypoglykämien,
- Hypoglykämie-Wahrnehmungsstörungen,
- eine Erkrankung oder Beeinträchtigung, die eine selbstständige kapilläre Blutglukosemessung nicht ermöglicht.
Die Leitliniensynopse stützt den Einsatz von CGM bei Menschen mit T2D insgesamt deutlich, jedoch mit klaren Einschränkungen hinsichtlich Zielgruppe und Evidenzqualität. CGM ist als eigenständiger Versorgungsaspekt im Kapitel 1.4.4 – K1 „kontinuierliches Glukosemonitoring (CGM)” innerhalb der Stoffwechselselbstkontrolle ausgewiesen. In nachfolgender Tabelle aus dieser Synopse wird dieser Aspekt als inhaltlich abweichend vom Standard der aktuell gültigen DMP-A-RL dargestellt:
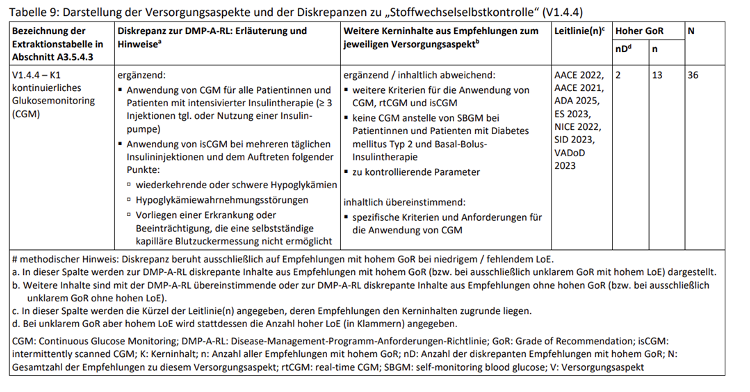
Würdigung des Evidenzgrades
Für intensiv insulinbehandelte und/oder hypoglykämiegefährdete Menschen mit T2D liegt überwiegend eine hohe oder zumindest solide Evidenz vor. Diese basiert auf randomisierten kontrollierten Studien (RCTs) und Metaanalysen und ist mit starken Empfehlungsgraden hinterlegt.
Für breitere Anwendungsbereiche – etwa den Einsatz von CGM bei weniger intensiv behandelten Menschen mit T2D oder primär „komfortorientierte“ Anwendungen – ist der Evidenzgrad hingegen überwiegend niedrig und beruht vor allem auf Expertenmeinungen.
Medizinisch-wissenschaftliche Argumente aus den Leitlinien
Die Leitlinien führen mehrere konsistente medizinisch-wissenschaftliche Argumente für den Einsatz von CGM bei ausgewählten T2D-Populationen an:
- Reduktion von Hypoglykämien: Der CGM-Einsatz bei insulinbehandelten Menschen mit T2D wird explizit mit der Prävention von Hypoglykämien sowie einer verbesserten Glukosekontrolle, unter anderem gemessen an der Time in Range, verknüpft.
- Verbesserte Therapiequalität bei intensivierter Insulintherapie: Für intensiv insulintherapierte Menschen ist der Nutzen von CGM in mehreren Leitlinien mit hohem Empfehlungsgrad und teils hohem Evidenzgrad belegt, insbesondere in Bezug auf HbA1c, Hypoglykämien und Glukosevariabilität.
- Unterstützung vulnerabler Gruppen: Bei Menschen mit eingeschränkter Hypoglykämiewahrnehmung oder bei PatientInnen, die kapilläre Blutglukosemessungen nicht sicher durchführen können, ermöglicht CGM in vielen Fällen überhaupt erst eine adäquate Stoffwechselselbstkontrolle.
Im Rahmen des Stellungnahme-Verfahrens zeigt sich ein klares Bild:
- Kein Stakeholder spricht sich explizit gegen den Einsatz von CGM aus.
- Mehrere Stellungnahmen empfehlen eine Aktualisierung zugunsten moderner rtCGM-Systeme sowie eine Anpassung an die Formulierungen der NVL 2023.
- Die geäußerte Kritik richtet sich nicht gegen CGM an sich, sondern gegen
- eine Übergewichtung von Empfehlungen mit schwacher Evidenz sowie
- veraltete oder nicht an die deutsche Versorgungspraxis angepasste Formulierungen, insbesondere mit Fokus auf isCGM.
Die Leitliniensynopse zeigt insgesamt eine klare Diskrepanz zwischen der aktuellen DMP-Regelung und dem Leitlinienstandard beim Einsatz von CGM auf. Für intensiv insulinbehandelte – definiert als mindestens drei Insulininjektionen pro Tag, was nicht der bisherigen ICT-Definition des G-BA entspricht – sowie hypoglykämiegefährdete Menschen mit T2D stellt CGM heute in zahlreichen Leitlinien einen evidenzbasierten Versorgungsstandard dar. Diese Nutzergruppen sollten daher im DMP ausdrücklich für den Einsatz von CGM vorgesehen werden.
Fazit: Bei erwachsenen Menschen mit T2D und intensivierter Insulintherapie (ICT/CSII) sollte CGM als kontinuierliches Glukosemonitoring eingesetzt werden. Bei patienten-individuellen Risikokonstellationen, insbesondere bei mehreren täglichen Insulininjektionen in Kombination mit einem erhöhten Hypoglykämierisiko, einer Hypoglykämiewahrnehmungsstörung oder einer eingeschränkten Fähigkeit zur Selbstmessung der Blutglukose (SMBG) – sollte der Einsatz von CGM erwogen werden. Die Dokumentation der Therapieergebnisse erfolgt dabei standardisiert anhand etablierter CGM-Metriken wie Time in Range (TIR), Time Below Range (TBR) und Time Above Range (TAR).
Die deutlich positiven Aussagen zum Einsatz von CGM bei Menschen mit T2D und Insulintherapie in den aktualisierten SoC der ADA dürften dazu beitragen, dass künftig mehr Healthcare Professionals – insbesondere auch Hausärztinnen und Hausärzte – in den USA CGM für diese Nutzergruppe verordnen. Ob die klare Positionierung der amerikanischen Fachgesellschaft mittel- bis langfristig auch zu Veränderungen in der Kostenübernahme durch die gesetzlichen Krankenkassen in Deutschland führen wird, bleibt abzuwarten. Wünschenswert wäre es!
Kernbotschaft: CGM ist für definierte Gruppen von Menschen mit T2D heute ein evidenzbasierter Versorgungsstandard – das DMP-Typ 2 sollte dies abbilden. Dabei gilt dies nicht nur für Menschen mit T1 und T2 Diabetes mit ICT-Therapie, sondern für alle Menschen mit Diabetes und Insulintherapie, egal ob ICT, BOT, SIT und CT. Es stehen inzwischen RCTs und auch zunehmend Outcome Studien zur Mortalität auch für Typ-2-Diabetes und Basalinsulintherapie (BOT) zur Verfügung. Leider wird in der Argumentation und Evidenzinterpretation für CGM hauptsächlich der „Insulinmanagement“ Part beachtet, während der Lebensstil und das Therapiemanagement zur „Selbstbefähigung“, d.h. Handeln im Sinne von Lebensstiladaption, vernachlässigt wird.
Obwohl wir die Evidenz und das Verständnis, was der Einsatz von CGM bewirken kann, aus vielen Untersuchungen kennen, wird dies leider ignoriert und nicht in medizinische und klinische Empfehlungen und Leitlinien umgesetzt. Die Ablehnungen der Kostenträger hinsichtlich Erstattung und auch die Einbeziehung des MDK, die fast immer ablehnen, geschieht dabei noch „on top“ innerhalb der vom G-BA gewährten Erstattung bei Typ-1 und Typ-2-Diabetes, fast immer aus formalistischen Gründen.
Warum ist Handeln notwendig?
- Die Evidenzlage hat sich seit dem G-BA-Beschluss 2016 grundlegend verändert.
- Internationale Leitlinien und die aktuelle IQWiG-Leitliniensynopse bestätigen den klinischen Nutzen von CGM bei intensiv insulinbehandelten und Hypoglykämie-gefährdeten Menschen mit T2D.
- Das aktuelle DMP bildet diesen Stand nicht ab und erzeugt Versorgungsungleichheiten.
Was ist fachlich konsentiert?
- CGM verbessert HbA1c, Time in Range und reduziert Hypoglykämien.
- Kein relevanter Stakeholder spricht sich gegen CGM aus.
- Kritik richtet sich ausschließlich gegen veraltete Definitionen und unklare Regelungen.
Was ist zu tun?
- Aufnahme von CGM in das DMP-Typ 2 für klar definierte Zielgruppen.
- Orientierung an der IQWiG-Leitliniensynopse als maßgeblicher fachlicher Grundlage.
- Schaffung von Rechtssicherheit für Leistungserbringer, Kostenträger und PatientInnen.
- Es braucht Sicherung in den bestehenden, empfohlenen Segmenten und Versorgungssicherheit für die Patienten und den verordnenden Ärztinnen.
- Seitens der ExpertenInnen und Fachgesellschaften braucht es eine Aktualisierung der Empfehlungen/Leitlinien entsprechend der bestehenden Evidenz für alle Menschen mit Diabetes, die mit Insulin behandelt werden.
- Last but not least folgt die Versorgung mit den Konzepten und Verhandlungen unter Berücksichtigung der wirtschaftlichen Aspekten.
Nutzen:
Das würde zu mehr und besserer Versorgungsqualität mit weniger regionalen Unterschieden sowie evidenzbasierten Entscheidungen führen.
Dieser Artikel erscheint als Teil des wöchentlichen Letters zu hochaktuellen Entwicklungen im Bereich Diabetes Technologie. Nutzen Sie das nebenstehende Formular um sich für den diatec weekly Newsletter anzumelden!
Mit freundlichen Grüßen
![]()

